مانند بسیاری از اکتشافات پیشگامانه، جداسازی سلولی(cell sorter) شروعی ساده داشت. ریشههای آن در تغییر داخلی یک شمارنده Coulter بود که در ابتدا برای شمارش سلولها به نوعی مرتبکننده سلول توسط مک فولویلر در آزمایشگاه لوس آلاموس استفاده میشد. راهاندازی او از همان فناوری برای جداسازی انواع مختلف سلولها استفاده میکرد. بر اساس تفاوت در مقاومت الکتریکی، که متناسب با تفاوت در حجم آنها بود، از یک جریان مایع عبور کرد. او آن را تغییر داد تا جریان مایع را به قطرات جداگانه تقسیم کند و سلول ها را بر اساس بارهای الکتریکی آنها دسته بندی کرد.
لئونارد “لن” هرزنبرگ، یک متخصص ژنتیک در استنفورد و یک نابغه با روحی تسلیمناپذیر، این دستهبندی سلولی ساده را که توسط ماک فولویلر ساخته شده بود، تغییر داد و آن را به چیزی تبدیل کرد که به FACS تبدیل میشود، فناوری که زیستپزشکی، تحقیقات ایمنیشناسی، و تشخیص بیماریها و بیماریها را متحول میکند. نظارت در سال های آینده محققان ایمونولوژی در آن زمان، از جمله لن، از ایمونوفلورسانس برای شمارش دقیق سلولهای رنگآمیزی فلورسنت زیر میکروسکوپ در یک اتاق تاریک استفاده میکردند. لن که میخواست ایمونوفلورسانس را با فلوسایتومتری برای شناسایی و جداسازی سلولها ترکیب کند، از فناوری جداسازی سلولی Fulwyler استفاده کرد، آن را با تکنیک چاپگر جوهر افشان توسعهیافته توسط ریچارد سویت در استنفورد ادغام کرد و یک مرتبکننده سلولی ساخت که قادر به شناسایی و جداسازی سلولها بر اساس سطح سلول است. نشانگرهایی با آنتیبادیهای رنگآمیزی فلورسنت برچسبگذاری شدهاند. او بهجای بارهای الکترواستاتیکی، از منبع نوری استفاده کرد که امکان تشخیص سلولهای طحال موش ایمنشده با سلولهای تخمدان همستر چینی (CHO) را فراهم کرد. او از رنگ فلورسئین دی استات برای برچسب زدن نشانگرهای زیستی استفاده کرد و در سال 1969، طحالهای تولیدکننده آنتیبادی را از سلولهای CHO بر اساس فعالیت فلورسانس افتراقی با استفاده از FACS (مرتبساز سلول فعال شده با فلورسانس) با موفقیت دستهبندی کرد. آنالایزرها، فناوری FACS و امکان اکتشافات علمی آن، به سرعت تکامل یافته است.
تکامل فناوری فلوسایتومتری
چگونه ابزار دقیق فلوسایتومتری از یک ابزار معمولی با صفحه نمایش اسیلوسکوپ و دوربین های پولاروید به فلوسایتومترهای پیشرفته امروزی تبدیل شدند؟
چگونه از آزمایشگاههای تحقیقاتی به کلینیک و حتی به ایستگاه فضایی بینالمللی منتقل شد؟
این تکامل نیازمند همکاری بین ذهنهای علمی خارقالعاده، مانند ذهن لن هرزنبرگ در استنفورد، و تجاریسازی و تخصص مهندسی برنی شور، از شرکتی مانند BD بود. این همکاری پنجاه سال پیش باعث راهاندازی فلوسیتومتر تجاری FACS – BD FACS II Cell Sorter – توسط BD Biosciences شد. دستهبندی سلولی BD FACS II توسط Becton & Dickinson Immunocytometry Systems (در حال حاضر BD Biosciences)، همراه با جانشینان خود، اکتشافات علمی در زمینه ایمونولوژی و پزشکی را در سالهای آتی منتشر خواهند کرد. واقعیت جالب: اصطلاح FACS توسط BD در سال 1985 علامت تجاری شد و BD FACS II Cell Sorter در حال حاضر بخشی از مجموعه موسسه Smithsonian است.
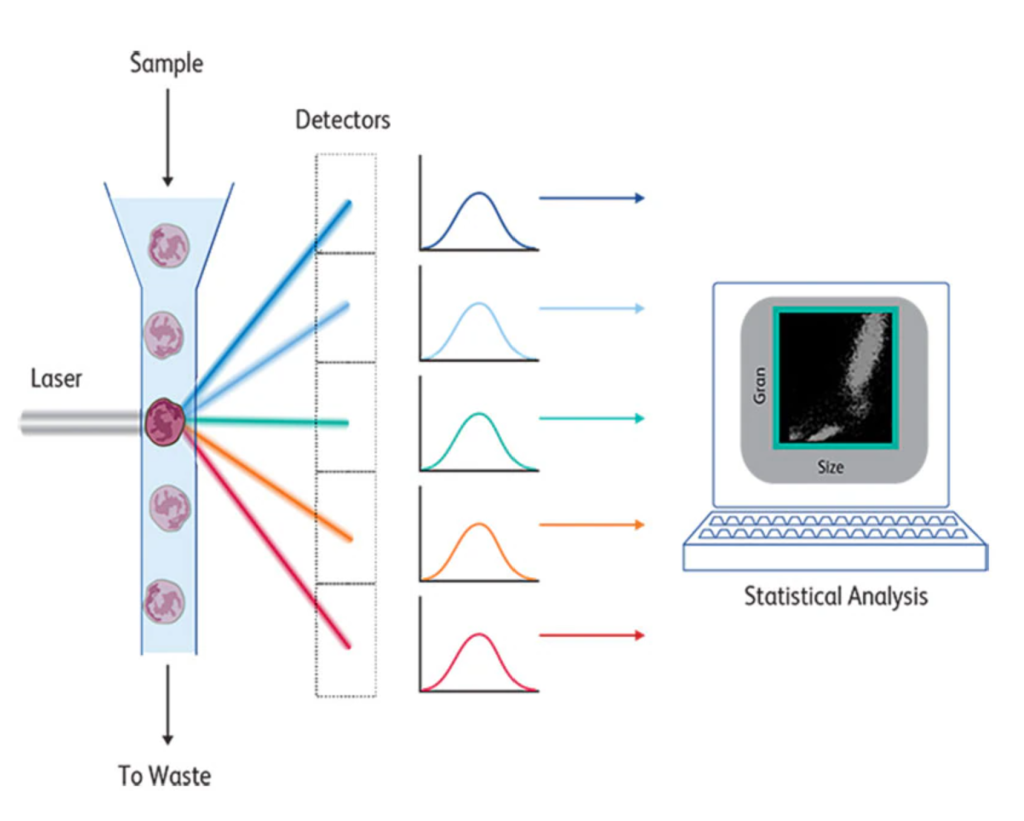
یک ابزار FACS نور ساطع شده از سلول های رنگ آمیزی شده توسط مولکولهای فلورسنت را که توسط لیزر در محدوده خاصی برانگیخته شده و در محدوده متفاوتی ساطع می کنند، اندازه گیری میکند. این طیفهای انتشار توسط آشکارسازها و فیلترهایی با پهنای باند مناسب جمعآوری میشوند تا پیک انتشار این فلوئوروکرومها را شناسایی کنند. سلولها یک به یک از پرتو لیزر برای تجزیه و تحلیل فردی به دنبال تمرکز هیدرودینامیکی بر اساس ویژگی های دینامیکی جریان آرام کواکسیال، که در سال 1883 توضیح داده شد، عبور می کنند. رنگ فلورسئین تغییر این لیزر به لیزر کریپتون، تشخیص فلورسانس دو رنگ را با استفاده از فلورسین و رودامین فعال کرد، که بعداً توسط BD به عنوان فلوسیتومتر BD FACS IV تجاری شد. در دهه 1980، لیزرهای کریپتون برای اولین بار با لیزر هلیوم-نئون و در نهایت با لیزرهای حالت جامد جایگزین شدند.
همانطور که بیولوژی و عملکرد سلول های ایمنی بیشتر مورد بررسی قرار گرفت، ایمونولوژیست ها شروع به درک ماهیت پیچیده سلولهای ایمنی کردند. لکوسیتها پروتئینهای متعددی را بیان میکنند و زیرجمعیتهای عملکردی مجزا را تشکیل میدهند. برای شناسایی این زیرمجموعه های ایمنی مختلف و تجزیه و تحلیل پیامدهای عملکردی آنها، تجزیه و تحلیل پارامترهای بالا ضروری بود، اما برای دستیابی به آن، فناوری باید در چندین جبهه تکامل مییافت. در دسترس بودن رنگ های فلورسنت عامل محدود کننده اصلی بود. تنها چند آنتی بادی پلی کلونال در دسترس بود و اینها به دلیل تنوع در نتایج حاصل از لاتهای (lots) مختلف و واکنش متقابل آنها، چالشهای بیشتری را ایجاد کردند. خوشبختانه، با معرفی تکنیک هیبریدوما جدید، یک پیشرفت تکنولوژیکی برای تولید آنتی بادیهای خاص با سلولهای B تولیدکننده آنتیبادی که با سلولهای میلوم نامیرا ترکیب شدهاند، به تازگی توسط کوهلر و میلشتاین ساخته شده است. نشانگرهای زیستی و تشخیص قابل تکرار و قابل اعتماد، نوید زیادی را برای ادغام آنها در زمینه های دیگر نشان داد. هرزنبرگ از آنتی بادی های مونوکلونال تولید شده با استفاده از تکنیک هیبریدوما در FACS6 استفاده کرد و پتانسیل قابل توجه این ترکیب را برای باز کردن FACS برای تبدیل شدن به یک تکنیک قدرتمند برای تجزیه و تحلیل سلولی نشان داد. اما برای دستیابی به این امر، تولید تجاری آنتی بادی های مونوکلونال باید اتفاق می افتاد.
مرکز مونوکلونال و تکامل معرف ها و ابزار دقیق فلوسایتومتری
ادامه همکاری بین لن هرزنبرگ از استنفورد و برنی شور از BD Biosciences منجر به تأسیس مرکز مونوکلونال BD شد که از عرضه مداوم معرفهای قابل اعتماد مورد نیاز برای تحقیقات مبتنی بر FACS اطمینان حاصل کرد. در اوایل دهه 70، فلورسین و رودامین تنها دو رنگ فلورسنت بودند که برای نشانگذاری نشانگرهای زیستی در دسترس بودند. با معرفی منابع لیزری اضافی در محدوده نور UV، بنفش و آبی، تجزیه و تحلیل نشانگرهای دخیل در چرخه سلولی و تجزیه و تحلیل کروموزوم ممکن شد. لیزرهای نئون هلیوم استفاده موثر از جلبکها و مولکولهای مشتق از سیانوباکتریها را که قادر به جذب انرژی نور و انتقال به مولکول های فلورسنت مانند فایکواریترین (PE) و آلوفیکوسیانین (APC) هستند در FACS امکان پذیر کرد. یک دنیای کاملا جدید برای تجزیه و تحلیل فلوسایتومتری با پارامترهای بالاتر جمعیت های سلولی پیچیده است.
در سال 1985، BD Biosciences BD FACScan Flow Cytometer را معرفی کرد، اولین ابزار تجاری با قابلیت اندازه گیری سه رنگ به طور همزمان، این اجازه می دهد تا سلول ها تحت پنج بعد مختلف (شامل دو پارامتر پراکندگی مرتبط با ویژگی های فیزیکی مانند اندازه، شکل و پیچیدگی) ارزیابی شوند. علاوه بر این، این اولین ابزاری بود که تراز ثابت را با کووتهای کوارتز معرفی کرد که نیاز به تنظیمات روزانه لیزری دستی توسط اپراتور ابزار را از بین برد. اولین فلوسایتومتر چهار رنگ، BD FACScan Flow Cytometer، تکامل خود را از اندازه گیری سه تا 10 پارامتر در بازه زمانی یک دهه تجربه کرد، به عنوان مثال، امکان تجزیه و تحلیل همزمان عملکرد و فنوتیپ جمعیت سلول های ایمنی را فراهم کرد. کمی سازی درون سلولی سیتوکینها توسط زیر مجموعه های سلولی ایمنی مشخص شده است.
همراه با افزودن تعداد بیشتری از پارامترهای قابل اندازه گیری، مسئله دیگری که باید به آن توجه می شد، اندازه بسیار زیاد فلوسیتومترها و نگهداری آنها بود. تلاشها برای کوچکسازی تنظیمات منجر به راهاندازی فلوسایتومتر BD FACSCalibur در سال 1995 شد، ابزاری فشردهتر و رومیزی که قادر به انجام تجزیه و تحلیل و جداسازی سلول است و فضای آزمایشگاهی را برای محققان آزاد میکند. این ابزار همچنین شامل گزینه هایی مانند BD FACS Loader و BD High Throughput Sampler برای اتوماسیون، و همچنین یک نرم افزار تخصصی برای اجرای برنامه های مختلف
می باشد.
معرفی خطوط لیزر قرمز، برچسبگذاری ایمنی با رنگهای سیانین و توسعه رنگهای tandem مانند
PE-Texas Red، PE-Cy5، PE-Cy5.5 و PE-Cy7.8 را امکانپذیر کرد. آرایهای از این رنگها برای ساختن 8 مورد استفاده قرار گرفت. رنگ، پانل فلوسایتومتری 10 پارامتری برای روشن کردن ناهمگنی لکوسیتها. رنگ های tandem مبتنی بر APC و رنگ های آلی کوچک نیز به صورت تجاری در دهه 1990 معرفی شدند، همراه با رنگ های مبتنی بر نانوکریستال های نیمه هادی که امکان جریان 18رنگ فلوسایتومتر را فراهم می کرد.
علاوه بر اینکه اکنون قادر به ارزیابی همزمان نشانگرهای سطحی بیشتری هستیم، در دسترس بودن همه این فلوئروکرومهای جدید تأثیر مستقیمی بر توسعه معرفها و سنجشهای جدید و سنجشهای ایمنی مبتنی بر مهره به نام Cytometric Bead Array داشت. این سنجش ها به ترتیب با شناسایی نشانگرهای فسفوریلاسیون داخل سلولی و کمی سازی سیتوکین های ترشح شده، درک بهتری از عملکرد سلول را امکان پذیر کردند.
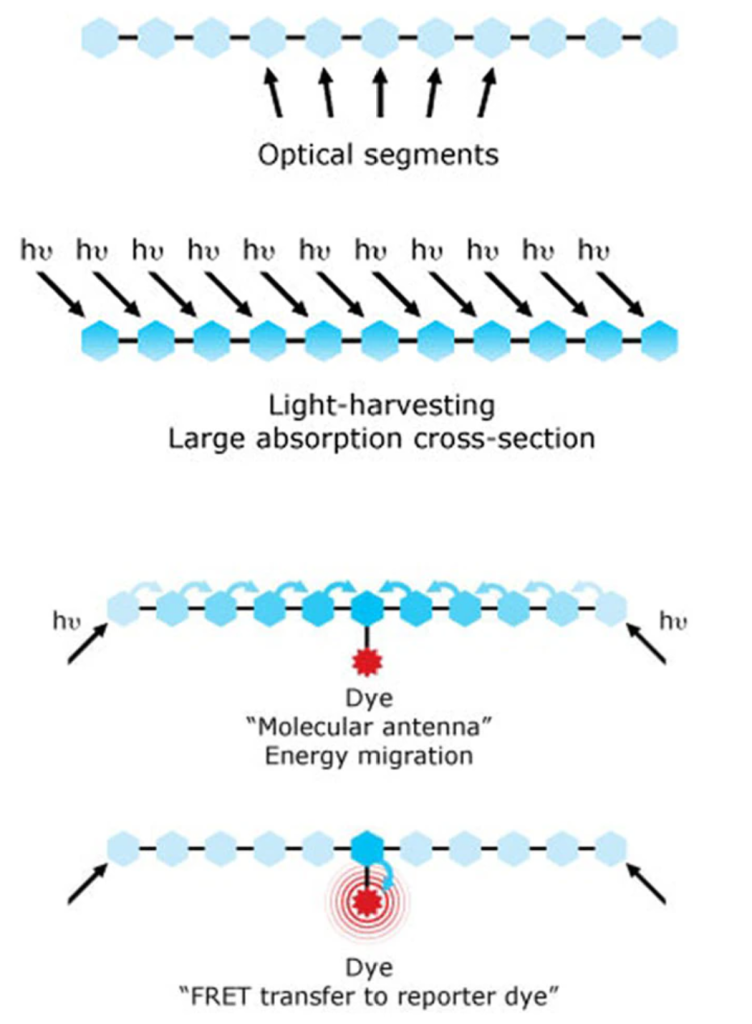
علیرغم انفجار همه این گزینههای رنگ، توانایی این رنگها برای جذب مؤثر نور عمدتاً محدود بود و بر حساسیت سنجشها تأثیر میگذاشت. این با استفاده از شیمی پلیمر رسانا که در سال 2000 جایزه نوبل را دریافت کرد، حل شد. رنگهای پلیمری جدید توسط Sirigen با استفاده از یک کلاس منحصر به فرد از پلیمرهای رسانا که به عنوان آنتنهای مولکولی عمل میکردند، ایجاد شد، که تغییرات روشن جدیدی از رنگها را امکانپذیر کرد. در سال 2014 BD Biosciences ، Sirigen را خریداری کرد و این فناوری را برای توسعه رنگهای بنفش و فرابنفش BD Horizon Brilliant پیادهسازی کرد که با گزینههای رنگ روشنتر، چشمانداز ایمونوفنوتایپینگ را تغییر داد.
به موازات آن، قابلیتهای ابزار دقیق با سرعتی سریع در حال پیشرفت بودند. BD چندین آنالیزگر و جداکننده سلولی را معرفی کرد. جالب است که یکی از این ابزارها، BD FACSVantage Flow Cytometer، به موزه تاریخ پزشکی و نوآوری پل اس. راسل، بیمارستان عمومی ماساچوست منتقل شده است تا از آن در تحقیقات پیشرفته در مورد پیوند اعضا استفاده شود. اولین سفارش ویژه 7 لیزری (پیکربندی شده برای مطابقت با نیازهای تحقیقاتی خاص کاربران) BD LSR II Flow Cytometer در سال 2008 به بسیاری از اکتشافات علمی کمک کرده است. معرفی یک ابزار سفارشی دیگر، BD LSRFortessa X-20 Cell Analyzer، که با BD Horizon Brilliant™ Violet Dyes و BD FACSDiva نرم افزار سازگار بود، تجزیه و تحلیل 20 پارامتر را به طور همزمان امکان پذیر کرد. علاوه بر آنالایزرهای سلولی با پارامترهای بالاتر،BD مرتبکنندههای سلولی سادهشدهای مانند BD FACSAria Cell Sorter را نیز معرفی کرد. این اولین فناوری بود که جداسازی قطرات الکترومغناطیس را با لیزرهای تراز ثابت به یک سلول جریان کووت جفت شده با ژل ترکیب کرد، عملکرد و تجربهای مشابه با آنالایزر سلولی ارائه داد و همچنین اتوماسیون دگرگونکننده را در جریان کار جداسازی با BD FACS Accudrop و Sweet Spot معرفی کرد. فناوریها، دستهبندی سلولی را برای محققان در دسترستر میسازد.
در دهه 2010، نوآوری به پیشبرد تکامل ابزارها در BD Biosciences ادامه داد. با اجرای فرآیندهای خودکار، مرتبکنندههای رومیزی قابلیت جداسازی سلولی را گسترش دادند، در حالی که هنوز امکان دسترسی آسان به محققان را فراهم میکردند. این دستاورد به طور کلی منجر به توسعه ابزارهای کوچکتر و خودکارتر شد، از جمله BD FACSVerse Flow Cytometer و BD FACSMelody Cell Sorter.
در عین حال، اهمیت استانداردسازی روشها، حذف فرآیندهای دستی و ناسازگاریهای جریان کار بین و درون آزمایشگاهها، که برای آزمایشگاههای بالینی که قابلیت تکرارپذیری و قابلیت اطمینان از اهمیت بالایی برخوردار است. حیاتی است. تکامل فلوسایتومترهای بالینی را با این قابلیتها تسریع کرد. معرفی اتوماسیونی که از فرآیندهای استانداردتر پشتیبانی می کند، نیاز به نسل بعدی فلوسایتومترهای بالینی، مانند فلوسایتومتر BD FACSlyric، ادغام شده با سیستم آماده سازی نمونه ممتاز FACSDuet را ایجاد کرد که کارایی جریان کار و نتایج مورد نیاز برای آزمایشگاه های بالینی را ارائه می دهد. تکامل جفتی آنالایزرها و مرتبکنندهها، همراستا با توسعه گزینههای جدیدتر فلوروکروم برانگیختهشده با لیزر UV، رنگهای فرابنفش BD Horizon Brilliant، همچنین منجر به معرفی خانواده جدیدی از ابزارهای با پارامتر بالا برای پشتیبانی از آزمایشهای چند رنگی رشتههای مختلف از جمله ایمونولوژی و ایمنی-انکولوژی شد.. آنالایزر سلولی A3 BD FACSymphony و آنالایزر سلولی BD FACSymphony A5 و دستهبندی سلولی BD FACSymphony S6 توانایی تولید دادههای فلوسایتومتری 30 پارامتری و فراتر از آن را با استفاده از رویکرد مرسوم استفاده از آشکارسازهای PMT منفرد فیلتر شده برای ارزیابی و ارزیابی فلوروکرومهای خاص ارائه میکنند.
تکامل نرم افزار فلوسایتومتری
یکی دیگر از عوامل محدود کننده سرعت در تکامل فلوسایتومتری نیاز به نرم افزار هوشمندتر بود که تجزیه و تحلیل تمام داده های فلوسایتومتری چند پارامتری را امکان پذیر می کرد. تجزیه و تحلیل دادههای فلوسایتومتری معمولی مستلزم گیتبندی دستی مناطق و نیاز به تجزیه و تحلیل ترکیبی از پارامترهای مختلف است. در ابتدا که تنها چند پارامتر اندازهگیری میشد، این کار نسبتاً ساده بود و میتوانست با استفاده از نمودارهای دو بعدی ساده انجام شود. اما با افزایش تعداد فلوئوروکرومها و در نتیجه تعداد پارامترهایی که میتوان اندازهگیری کرد، تعداد نمودارهای دوبعدی بهطور تصاعدی افزایش یافت و تجزیه و تحلیل دادهها را بسیار پیچیده کرد. محدودیتهای نرمافزار موجود مانع از گسترش تعداد پارامترهای قابل اندازهگیری در 15 سال اول پس از معرفی FACS در دهه 1970 شد.
به طور کلی، فلوسایتومترها به نرم افزارهای مخصوص ابزار مجهز هستند، مانند نرم افزار BD FACDiva که در سال 2002 معرفی شد، که در حال حاضر از ده فلوسیتومتر BD پشتیبانی می کند! علاوه بر نرم افزارهای تعبیه شده در ابزارها، در طول دهه 1990، نرم افزارهای مستقلی مانند نرم افزار FlowJo معرفی شدند. این نرمافزار قابلیتها و گزینههای تحلیلی را ارائه میکند که میتواند انعطافپذیری و قدرت را به تجزیه و تحلیل دادههای فلوسایتومتری اضافه کند، در نتیجه از پیشرفتهای مستمر آن در جهت ارائه پارامترهای داده بیشتر و امکان ابعاد تحلیلی بیشتر هر سلول پشتیبانی میکند. در طول سالها، نرمافزار FlowJo بهطور مداوم با پیروی از همان ریتم تکامل سازها تکامل یافته است. با نزدیک به سه دهه و 10 نسخه اصلی، نرمافزار FlowJo ابزار آگنوستیک سازگار شده است تا از تغییرات ثابت فایلهای تولید شده توسط نسلهای جدیدتر فلوسایتومترها پشتیبانی کند و در عین حال راههای جدیدتری برای تجزیه و تحلیل، تفسیر، تجسم و نمایش دادهها ارائه دهد. در حال حاضر، این نرم افزار در خط مقدم ترکیب رویکردهای کاهش ابعاد مانند tSNE و UMAP به میدان فلوسایتومتری به عنوان وسیله ای برای پشتیبانی از داده های با پارامترهای بالاتر معرفی شده توسط جدیدترین فناوری ها قرار دارد که به محققان اجازه می دهد پاسخ های خود را سریعتر از قبل پیدا کنند.
ظهور فلوسایتومتری full spectrum
روش متفاوتی برای تجزیه و تحلیل سلولی با استفاده از فلوسایتومتری طیفی در دهه های گذشته شتاب بیشتری به دست آورده است. فناوری فلوسایتومتری full spectrum برای اولین بار در سال 2004 در کنگره انجمن بین المللی سیتولوژی تحلیلی معرفی شد و از آن زمان تاکنون تکامل یافته است. برخلاف فلوسایتومترهای معمولی که تنها بخش مجزایی از طیف انتشار را که توسط یک فیلتر و آشکارساز در هر فلوئوروکروم تعریف میشود جمعآوری میکنند، فلوسیتومترهای full spectrum کل طیف مرئی را با حداقل شکاف جمعآوری میکنند. طیف انتشار هر فلوئوروکروم توسط آرایه ای از آشکارسازهای فیلتر شده جمع آوری می شود. یک الگوریتم غیر اختلاط طیفی برای تعیین سهم فلوئوروکرومهای منفرد استفاده میشود و آن را از الگوریتمهای سنتی مورد استفاده برای جبران در فلوسیتومترهای معمولی متمایز میکند. آنالایزر سلولی Symphony A5 SE با قابلیت طیفی، که توسط BD در سال 2021 معرفی شد، توانایی به دست آوردن پوشش کامل طیف مرئی را ارائه می دهد و امکان اندازه گیری بیش از 40 رنگ (تا 50 پارامتر) را فراهم می کند که فلوسایتومتری معمولی و طیفی را امکان پذیر می کند. توسعه همزمان فلوروکرومهای فعال طیفی، مانند رنگهای BD Horizon RealYellow و BD Horizon RealBlue، که برای کاهش سرریز طراحی شدهاند، قدرت تجزیه و تحلیل سلولی را با استفاده از فلوسایتومتری طیفی افزایش داده است. در سال 2023، این تکامل منجر به معرفی جدیدترین فناوری از BD برای تجزیه و تحلیل طیفی شد. فناوری BD SpectralFX، موجود در دستهبندی سلولی BD FACSDiscover™ S8، تجزیه و تحلیل سلولهای طیف کامل و جداسازی را از طریق 78 آشکارساز APD فلورسانس همراه با پهنای باند فیلتر بهینهسازی الگوریتمی ممکن میسازد.
سایتومتری تصویربرداری (Image cytometry)
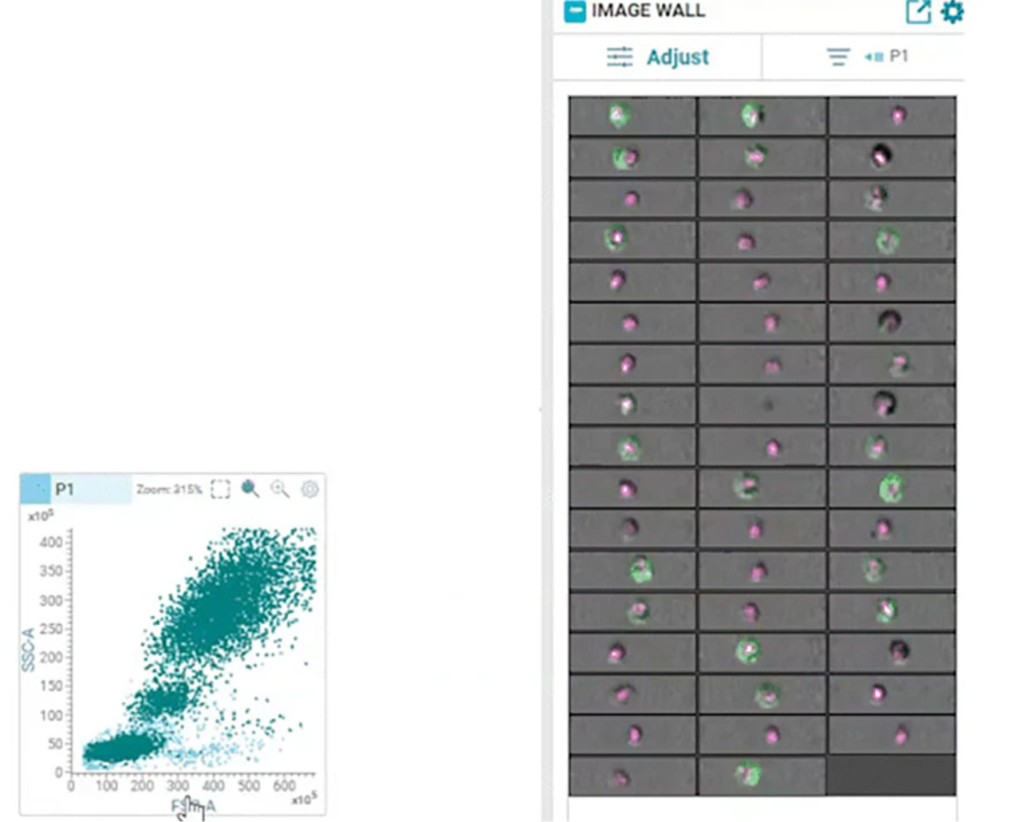
تجزیه و تحلیل دادههای چندپارامتری میتواند بینشهای مهمی بر اساس شدت سیگنالهای فلورسانس در مناطق گیتبندی شده در نمودارهای کانتور دو بعدی به دست آورد. با این حال، این رویکرد فاقد وضوح فضایی است که می توان از تصویربرداری از سلول های منفرد به دست آورد و مستعد به دست آوردن نتایج اشتباه با ناتوانی در تمایز بین دوتاییها، باقی ماندهها و سلولهای منفرد واقعی است. علاوه بر این، جایگیری درون سلولی بیومارکرهای پروتئینی را نمی توان به راحتی با این تکنیک اندازه گیری کرد. سایتومتری تصویربرداری به برخی از این مسائل پرداخت. فلوسایتومتری را با تصویربرداری ترکیب کرد و تصویربرداری از سلول های منفرد را فعال کرد، اما نمی توان آن را با جداسازی با سرعت بالا ترکیب کرد. ترکیب تصویربرداری بیدرنگ از سلولها و جداسازی با سرعت بالا و توان عملیاتی، برای چندین دهه رویایی محقق نشده باقی مانده بود.
در سال 2022، BD Biosciences با راهاندازی فناوری تصویر پیشگامانه BD CellView که تصویربرداری فوقسریع از سلولها را همراه با جداسازی سلولی با سرعت بالا امکانپذیر میکند، این رویا را به واقعیت تبدیل کرد. این فناوری از فناوری صنعت ارتباطات بی سیم برای به دست آوردن تصاویر فلورسنت چند رنگ در زمان واقعی استفاده می کند و از آن اطلاعات برای جداسازی سلول ها با سرعت حداکثر 15000 رویداد در ثانیه استفاده می کند!
در سال 2023، این فناوری با فناوری BD SpectralFX ترکیب شد، که جداسازی سلولهای طیفی کامل را امکانپذیر میسازد تا اولین مرتبکننده سلول طیفی تصویربرداری در لحظه در نوع خود ایجاد شود: دستهبندی سلول BD FACSdiscover S8. این ترکیبی از فلوسایتومتری طیفی با بینشهای فضایی و مورفولوژیکی در لحظه (RTI-SFC)، همراه با معماری نوری مدولار جدید و الگوریتمهای آگاه از سیستم، دریچهای را برای امکانات بی حد و حصر برای دانشمندان باز کرده است.
پیش بردن مرزهای علم و پزشکی با FACS
از زمان معرفی FACS در دهه 1970 تا پنج دهه پس از آن، قدرت باورنکردنی استفاده از آن در تجزیه و تحلیل چندپارامتری با ابعاد بالا برای تشخیص، شمارش و جداسازی زیرجمعیتهای سلول ایمنی محقق شده و استفاده از آن در محیطهای بالینی تبدیل شده است. یکی از اولین زمینه هایی که از آن بهره مند شد، تحقیقات HIV بود. در دهه 1980، در اوج شیوع ایدز، FACS در تشخیص بالینی و متعاقباً برای ارزیابی و پایش HIV گنجانده شد. فلوسایتومتری در اثبات این که کاهش سلول های +CD4 نشانه اصلی عفونت HIV است، بسیار مفید بود. فلوسایتومتری سه رنگ برای اندازه گیری سلول های سیتوتوکسیک +CD4 و +CD8 کاربرد بالینی این تکنیک را تسهیل کرد. حجم باورنکردنی تحقیقات بعدی از فلوسایتومتری برای شناسایی نشانگرهای سلولهای T فعال، سلولهای T اولیه، سلولهای T تنظیمکننده و عملکرد سلولهای T استفاده کرد. تعجبی نداشت که فلوسایتومتری بالینی برای اولین بار در مدیریت بیماران HIV استفاده شد. علاوه بر HIV، تحقیقات در مورد لوسمی و لنفوم نیز از استفاده از فلوسایتومتری در سالهای بعد سود زیادی برد. استفاده بالقوه از ذرات کوچک مانند وزیکول های خارج سلولی به عنوان نشانگرهای زیستی در سال های اخیر به طور گسترده مورد بررسی قرار گرفته است و پیشرفت در ابزار دقیق برای تشخیص ذرات کوچک، مانند آنچه که توسط BD FACSymphony A1 Cell Analyzer ارائه شده است، به دانشمندان کمک می کند تا مرزهای تحقیقات را پیش ببرند.

در چند دهه گذشته، زمینه رو به رشد ایمونوتراپی سرطان با پیشرفت سریعی که از اولی با توجه به کشف زیست شناسی پشت مهار ایست بازرسی ایمنی حاصل شد. پارادایم جدیدی در درمان سرطان با استفاده از رویکرد هدف قرار دادن مسیرهای بازدارنده ایجاد شد که یک پاسخ ایمنی موثر در برابر سرطان را مسدود می کرد. فلوسایتومتری نقش عمدهای در روشن کردن نقش پروتئین آنتی ژن 4 (CTLA-4) مرتبط با لنفوسیت T سیتوتوکسیک و گیرنده مهارکننده ایمنی PD-1 برای تقویت ایمنی ضد تومور ایفا کرد. جیمز آلیسون و تاسوکو هونجو، مغزهای علمی پشت این استراتژیها، جایزه نوبل فیزیولوژی و پزشکی را در سال 2018 دریافت کردند.
BD Biosciences با استفاده از چندین فلوسیتومتر BD، مانند BD FACScan، BD LSR II مفتخر بود که بخشی از سفر آنها بود. و BD FACSCalibur، در آزمایشات برجسته خود.
با این همه پیشرفت، ما تازه شروع به کشف آنچه که با استفاده از فلوسایتومتری ممکن است، داریم.

