مرگ سلولها از روشهای مختلف بدن را قادر میسازد که از سلولهای ناخواسته پاکسازی شود. مطالعات در طول سالها مکانیسمهای مولکولی مختلف و نتایج عملکردی چندین مسیر کلیدی مرگسلولی را بررسی کردهاند.
انواع مرگ سلولی
در حال حاضر، انواع مرگ برنامهریزیشده سلولی (PCD: Programmed cell death) که به شدت مورد بررسی قرارگرفتهاند شامل: آپوپتوز، نکروپتوز، پیروپتوز، فروپتوز، پانوپتوز، و اتوفاژی میباشد که نقش مهمی در تنظیم ریزمحیط تومور (TME: Tumor microenvironment) سرکوبکننده سیستم ایمنی، تعیین نتایج بالینی و رویکردهای درمانی سرطان ایفا میکند. مرگ سلولها از روشهای مختلف بدن را قادر میسازد که از سلولهای ناخواسته پاکسازی شود. مطالعات در طول سالها مکانیسمهای مولکولی مختلف و نتایج عملکردی چندین مسیر کلیدی مرگسلولی را بررسی کردهاند. در حال حاضر، انواع مرگ برنامه ریزی شده سلولی که به شدت مورد بررسی قرارگرفتهاند شامل: آپوپتوز، نکروپتوز، پیروپتوز، فروپتوز، پانوپتوز، و اتوفاژی میباشد که نقش مهمی در تنظیم ریزمحیط تومور سرکوبکننده سیستم ایمنی، تعیین نتایج بالینی و رویکردهای درمانی سرطان ایفا میکند.
برای حفظ هموستاز فیزیولوژیکی در حالتهای نرمال یا تحت فشاراسترس (آسیب یا عفونت و غیره)، سلولها مسیرهای مرگ سلولی متفاوتی را اتخاذ میکنند که نتایج مورفولوژیکی و عملکردی متمایز ایجاد میکند. در یک بزرگسال، تقریباً 50 تا 70 میلیارد سلول هر روز میمیرند تا گردش سلولی سالمی را حفظ کنند. PCD و non-PCD هر دو در این فرآیند شرکت میکنند. با این تفاوت که مرگ برنامهریزیشده توسط مسیرهای مولکولی دقیق تنظیم میشود، در حالی که non-PCD (مانند نکروز) به عنوان یک مرگ زودرس ناشی از آسیب شناخته میشود.
تقسیم بندی مرگ سلولی از نظر ایمونوژنیسته:
با توجه به توانایی شروع و تشدید پاسخ ایمنی اکتسابی، مرگ برنامهریزیشده را میتوان به دو دسته ایمنوژنیک (یا التهاب زا مثل نکروز) و غیرایمونوژنیک (یا تحملزا مثل آپاپتوز) طبقهبندی کرد. مرگ برنامهریزیشده سلولی ایمونوژنیک از طریق انتشار اجزایسلولی، عمدتاً سایتوکینهای پیشالتهابی یا سایر الگوهای مولکولی مرتبط با آسیب (DAMPs: Damage-associated molecular patterns)، به سیستمایمنی اطراف از خطر بالقوه هشدار میدهد. این سیگنالها توسط گیرندههای تشخیصالگو (PRRs: Pattern recognition receptors) در سلولهای ایمنیذاتی شناسایی میشوند، بنابراین پاسخهای ایمنی بعدی را فعال میکنند. از سوی دیگر، مرگسلولی غیرالتهابزا مانند آپوپتوز، یکپارچگی غشایسلولی را بدون نشت محتویات سلولی حفظ میکند، بنابراین منجر به پاکسازی توسط سلولهای فاگوسیتی بدون شروع التهاب بیشتر میشود «Silent».
اتوفاژی یک استراتژی حامی بقا میباشد که برای جلوگیری از مرگبرنامهریزیشده سلولی گسترده توسط سلولها اتخاذ میشود و میتواند تحت شرایط فیزیولوژیکی خاص به نوع دیگری از مرگ برنامهریزیشده سلولی تبدیل شود.
نکته: گرچه آپوپتوز به طور معمول غیرایمونوژنیک است، اما مطالعات نشان دادهاند که تحت شرایط خاص مانند کمبود کاسپاز، آپوپتوز میتواند با فعالکردن سیگنالینگ NF-kB و مسیر cGAS/STING، پاسخ های ایمنیاکتسابی ضدتوموری یا ضدویروسی را تحریک کند. علاوه براین، رادیوتراپی یا شیمیدرمانی میتواند آپوپتوز ایمونوژنیک را نیز القا کند.
آپوپتوز: مرگ سلولی به واسطه کاسپاز 3/7

یکی از اولین مرگهای برنامهریزیشده سلولی غیرایمونوژنیک که به خوبی شناخته شدهاست، آپوپتوز میباشد. تا به امروز، سه مسیراصلی برای فعالسازی آپوپتوز شرح داده شدهاست که شامل مسیرهای بیرونی، درونی و با واسطه پرفورین/گرانزیم میباشد. همه این مسیرها به زیبایی توسط برشهای متوالی پروتئازهای خاص آسپارتات (کاسپازها) به صورت زنجیرهای رخ میدهند و نهایتا منجر به فعالشدن کاسپاز-3 میشوند که واسطه القا مرگسلولی از طریق آسیبهای سلولی متعدد میباشد.
به عنوان مثال کاسپاز-3 با بریدنgelsolin و Rho effector protein ROCKI باعث سازماندهی مجدد اسکلتسلولی و تشکیل حبابهای آپوپتوز میشود. همچنین با بریدن XKR8 و غیرفعالکردن فاکتورهای کمپلکس فسفولیپید فیلیپاز( به وسیله بریدن ATP11A، ATP11C و CDC50a) باعث افزایش در معرض قرارگرفتن فسفاتیدیل سرین (PS) میشود.
بهطورکلی، آپوپتوز با ویژگیهای مورفولوژیکی نظیر انقباضسلولی، تکهتکهشدن کروماتین، ایجاد حبابغشایی، واکوئلاسیون سیتوپلاسمی و تجزیه به وزیکولهای غشاءدار به نام آپوپتوزم شناخته میشود. این تغییرات در نهایت باعث ازهمپاشیدگی سلولی میشود و به دنبال آن اجسام آپاپتوزوم با PS در غشاخارجی خود (که به عنوان نشانگر برای سلولهای فاگوسیتکننده عمل میکند) توسط سلولهای فاگوسیتکننده از محل خارج میشوند بدون اینکه محتویاتسلولی پیشالتهابی به محیط خارجسلولی آزاد شود.
آپاپتوز میتواند به مبارزه با بیماری خودایمنی و سرطان کمک کند و از طرف دیگر مهار آپوپتوز میتواند وقایع مختلف از پیری تا بیماری ایسکمیک قلبی و بیماری مغزی را کنترل کند.
انواع مسیرهای آپوپتوز:
سیگنالهای آپوپتوز خارج سلولی، مانند فاکتور نکروز تومور-آلفا (TNF-a)، منجر به فعالشدن گیرنده سطحسلولی آنها شده که در ادامه منجر به تشکیل یک کمپلکس پروتئینی چندجزئی در سمت سیتوزولی غشای پلاسمایی به نام کمپلکسI میشود. کمپلکسI از پروتئینهای آداپتور TRADD و TRAF2، گیرندهپروتئینکیناز-1 (RIPK1) و یکجفت لیگاز مهارکنندهکاسپاز (cIAP: Caspases inhibiting activity)، تشکیل شدهاست. کمپلکسI به طور معمول مسیرسیگنالینگ NF-KB را فعال میکند و باعث رونویسی سایتوکینهای مختلف و پروتئین های ضدآپوپتوز میشود. بعلاوه، کاسپاز-3 و کاسپاز-7 از طریق برش توسط کاسپازهای آغازگر، از جمله کاسپاز-8، در پاسخ به سیتوکینهای القاکننده مرگ سلولی از مسیر خارج سلولی فعال میشوند و اثرات خود را اعمال میکنند.
آپوپتوز مسیر داخل سلولی (وابسته به کاسپاز9) در پاسخ به اختلالات میکرو محیطی مختلف، از جمله آسیب DNA، استرس شبکهآندوپلاسمی (ER)، تجمع گونههای فعال اکسیژن (ROS) و کمبود فاکتور رشد آغاز میشود. این تغییرات منجر به اختلال در یکپارچگی غشای خارجی میتوکندری (MOM: Mitochondrial outer membrane) شده و باعث نشت برخی از پروتئین های میتوکندری مانند سیتوکرومc و Smac/Diablo میشود. سیتوکرومc به C-ترمینال Apaf-1 متصل میشود که یک ذره چرخ مانند هپتامر به نام آپوپتوزوم را تشکیل میدهد. Apaf-1 پروکاسپاز-9 را به آپوپتوزوم جذب میکند موجب فعال شدن کاسپاز-9 از طریق برش خودکار میشود.
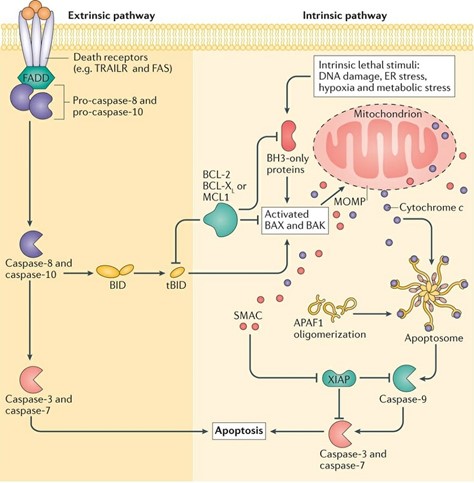
بنابراین، هر دو کاسپاز-3 و کاسپاز-7 از طریق برش توسط کاسپازهای آغازگر، از جمله کاسپاز-8، در پاسخ به سیتوکینهای القاکننده مرگ سلولی خارج سلولی و کاسپاز-9 در پاسخ به نفوذپذیری غشا خارجی میتوکندری (MOMP: Mitochondrial outer membrane permeabilization) فعال میشوند.
همانطورکه گفتهشد، مرحله اساسی مسیر آپوپتوز به واسطه کاسپاز-9، MOMP میباشد که به شدت توسط پروتئینهای خانواده BCL-2 کنترل میشود.
خانواده BCL-2 را میتوان با توجه به عملکرد آنها در آپوپتوز به سه گروه تقسیم کرد:
- گروه اول شامل BAX و BAK هستند که باعث MOMP میشوند.
- گروه دوم شامل اعضای ضدآپوپتوز شامل BCL-2، BCL-XL، BCL-W و MCL-1 است که مستقیماً به BAX و BAK متصل میشوند و به عنوان آنتاگونیست عمل میکنند.
- گروه سوم شامل اعضای proapoptotic، حاوی یک دومین BH3 (BH3-only) میباشند که شامل BIM، BID، BAD، PUMA و NOXA میشود. این پروتئینها در مرحله رونویسی یا پس از ترجمه بر اثر اختلال هموستاز سلولی فعال میشوند و به اعضای ضدآپوپتوز BCL-2 متصل میشوند تا برهمکنشهای مهاری آنها با BAX/BAK را کاهش دهند و به BAX/BAK اجازه میدهند الیگومرهایی را روی MOM تشکیل دهند تا آن را در برابر پروتئینهای فضای بین غشایی میتوکندری نفوذپذیر کنند.
نکته: مسیر آپوپتوز با واسطه کاسپاز-8 همچنین میتواند باعث فعال شدن MOM شود. بنابراین آپوپتوز میتوکندری از طریق برش BID توسط کاسپاز-8 نیز اعمال میشود.
BID یک پروتئین منحصر به فرد BH3-only است که پس از برش قسمت N ترمینال آن فعال میشود و موجب تولید BID کوتاه شده (tBID) میشود که قادر است به آسانی از سیتوزول به میتوکندری منتقل شود و MOM را تحریک کند.